~クライオ電子顕微鏡によってワニのヘモグロビンのもつ特徴的なアロステリック制御のしくみを解明~
横浜市立大学大学院生命医科学研究科 高橋捷也さん(博士後期課程3年)、ジェレミー・テイム教授、西澤知宏教授、李勇燦助教らの研究グループは、Aarhus大学(デンマーク)Angela Fago教授、Nebraska大学 Jay Storz教授、大阪大学蛋白質研究所 栗栖源嗣教授、川本晃大助教らとの国際共同研究により、ワニのヘモグロビンの立体構造とそのアロステリック制御
*1に関わる重炭酸イオンとの結合様式を、クライオ電子顕微鏡単粒子解析
*2により明らかにしました。
本研究成果は、科学誌「Nature Communications」に掲載されました(2024年8月2日)。
研究成果のポイント
- クライオ電子顕微鏡を用いて、ワニのヘモグロビンの立体構造とそのアロステリック制御に関わる重炭酸イオンの結合様式を解明しました。
- 重炭酸イオンの結合に重要な、ワニのヘモグロビンにおけるアミノ酸置換を特定しました。
- ヘモグロビンのような普遍的な分子が、生物の進化にともなって、どのように進化してきたのか、その関連性の理解に寄与することが期待されます。
研究背景
ヘモグロビンは血液中で酸素運搬の役割を担うタンパク質であり、全ての脊椎動物において共通の機能を果たします。ヘモグロビンはαサブユニットとβサブユニットがそれぞれ2つずつ会合した4量体構造をとります。各サブユニットはヘムと呼ばれる赤色に見える鉄イオン錯体をもっており、酸素が1分子結合することができます。酸素がヘムに結合すると、ヘモグロビン4量体はR (Relaxed) 型という「開いた」構造をとり、一方で、酸素が外れるとT (Tense) 型という「閉じた」構造をとることが知られています。これらの構造の変化は、ほとんどの脊椎動物において、有機リン酸の作用によってアロステリックに制御されます。一方、脊椎動物で唯一ワニは、有機リン酸の作用を受けることなく、重炭酸イオンの作用を受けることが40年以上前に報告されました。この重炭酸イオンの作用のおかげで、ワニは長時間潜水しても酸素を供給することができるため、それを活用した狩りを行うことが可能です。このワニに特有な重炭酸イオンの作用を明らかにするために、ワニのヘモグロビンの立体構造の分子レベルでの解析が必要でしたが、ワニのヘモグロビンは良質な結晶が得られておらず、いまだにX線結晶構造解析による構造決定に成功していません。そこで今回、研究グループはクライオ電子顕微鏡単粒子解析法を用いることで、ワニのヘモグロビンの構造決定を目指しました。
研究内容
研究グループは、North Texas大学にて生態学の実験目的で飼育されているワニ (
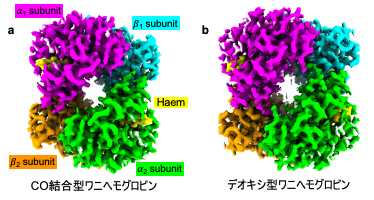
Alligator mississippiensis) から採取された血液からヘモグロビンを精製して、クライオ電子顕微鏡による構造解析を行いました。それにより、酸素が結合した状態、一酸化炭素 (CO) が結合した状態(図1a)、および酸素が解離した状態(デオキシ状態)(図1b)の3種類の状態の立体構造を明らかにすることに成功しました。デオキシ状態のヘモグロビン試料は、大阪大学栗栖研究室に設置された嫌気チャンバー内の低酸素環境下で調製しました。
図1 a) 一酸化炭素 (CO) が結合した状態のR型構造をとったワニのヘモグロビンの電顕マップ。b) デオキシ状態のT型構造をとったワニのヘモグロビンの電顕マップ。α1サブユニットをピンク色、β1サブユニットを水色、α2サブユニットを黄緑色、β2サブユニットをオレンジ色、ヘムを黄色で表示している。
・重炭酸イオンとの結合様式
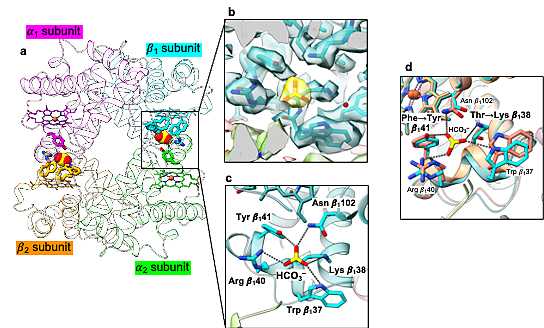
2.2オングストローム(Å、1Åは100億分の1メートル)の高分解能で決定した、T型構造をとったデオキシ状態のワニのヘモグロビンの立体構造から、ヘモグロビン4量体のαサブユニット、βサブユニットの界面に合計2分子の重炭酸イオンが結合することが明らかになりました(図2a)。その結合部位は、他の脊椎動物のヘモグロビンにおける有機リン酸の結合部位とは異なっており、ワニのヘモグロビンが独自に獲得したものであることがわかりました。重炭酸イオンは合計8つのアミノ酸によって認識されており(図2b、c)、ヒトを含む他の動物のヘモグロビンと比較すると、ワニでは特に2つのアミノ酸置換(βサブユニットの38番目のスレオニン
*3と、41番目のフェニルアラニン
*4)が重炭酸イオンによる作用を獲得するために重要であることが明らかになりました(図2d)。
図2 a) 重炭酸イオン(黄色)が結合したT型構造のワニのヘモグロビンの立体構造。b) 重炭酸イオンの電顕マップの密度。c) 重炭酸イオンとT型構造のワニのヘモグロビンのβ1サブユニット(水色)との結合様式。d) ワニのヘモグロビン(水色)とヒトのヘモグロビン(オレンジ色)における重炭酸イオン結合部位の比較。
今後の展開
この研究の起源は、実に40年以上前にさかのぼります。1977年に初めてワニのヘモグロビンの重炭酸イオン作用が報告されて以降、イギリス分子生物学研究所のMax Perutz博士や長井潔博士らによって、その仕組みが議論されてきましたが、立体構造は長い間明らかになっていませんでした。本研究は、これらの長い研究の末に実を結んだ成果であると言えます。
本研究により、ワニが進化の過程で独自に獲得した重炭酸イオン作用の仕組みが明らかになったことで、脊椎動物のヘモグロビン分子進化における新たな知見を提供できる可能性が期待されます。また、今後、鎌状赤血球症等で心肺機能の弱い患者に対する遺伝子治療や輸血用人工血液といった医療への応用も期待されます。
本論文の責任著者であるテイム教授(横浜市立大学大学院生命医科学研究科)をはじめ、複数の研究者の指導者でもあった故長井博士に特別の感謝を示したいと思います。
研究費
本研究は、文部科学省科学研究費助成事業(JP23H02439, JP24H02264[西澤])、JST次世代研究者挑戦的研究プログラム(JPMJSP2179[高橋])、AMED研究事業(JP23ama121001)の支援を受けて行われました。
論文情報
論文タイトル:The unique allosteric property of crocodilian haemoglobin elucidated by cryo-EM.
著者:Takahashi K, Lee Y, Fago A, Bautista NM, Storz JF, Kawamoto A, Kurisu G, Nishizawa T*, Tame JRH. * (*correspondence)
掲載雑誌:Nature Communications
DOI:
https://doi.org/10.1038/s41467-024-49947-x
用語説明
*1 アロステリック制御:ヘモグロビンの一つのサブユニットに酸素が結合すると、連鎖的に4量体の他のサブユニットにも構造変化が伝わり、酸素に対する親和性が向上する仕組み。この仕組みによって、ヘモグロビンにおける酸素結合・解離は協同的に起こることが知られている。
*2 クライオ電子顕微鏡単粒子解析 : クライオ電子顕微鏡と呼ばれる装置を用いて、約-180℃の低温環境下でタンパク質などの試料に電子線を照射して撮影し、得られた粒子像から三次元構造情報を再構成して、分子の立体構造を解析する手法。
*3 スレオニン(ヒトではリジン) : 20種類ある天然アミノ酸のうち、スレオニン、リジンはいずれも親水的ではあるが、スレオニンに対してリジンは側鎖が長く、先端にアミド基に由来する正電荷をもつ。ワニのヘモグロビンでは、リジンの正電荷が重炭酸イオンの負電荷とイオン結合を形成する。
*4 フェニルアラニン(ヒトではチロシン) : 20種類ある天然アミノ酸のうち、チロシンとフェニルアラニンはいずれもベンゼン環構造を側鎖にもつが、チロシンは側鎖の先端に水酸基が付加されている。ワニのヘモグロビンでは、チロシンの水酸基が重炭酸イオンと水素結合を形成する。