横浜市立大学大学院医学研究科 分子生物学の鈴木秀文助教、阿部竜太共同研究員(研究当時:医学部学生)、髙橋秀尚教授の研究グループは、メディエーター複合体*1のサブユニットMED26とLittle elongation complex (LEC) *2が、2つの核内凝集体*3Histone locus body(HLB)とCajal bodyを会合させることで、新規のRNAポリメラーゼII (Pol II)の一時停止を引き起こし、ヒストン遺伝子の発現を制御することを明らかにしました(図1)。
本研究成果は、英科学誌Nature Communicationsに掲載されました。(日本時間2022年5月25日18時)
研究成果のポイント
- メディエーター複合体と核内凝集体による新たな遺伝子発現制御機構が明らかとなった。
- MED26とLECが、ヒストン遺伝子の転写の最終段階でPol IIの一時停止を引き起こすことが明らかとなった。
- 腫瘍性疾患の進展に関与するヒストン遺伝子の発現を制御する仕組みの一端が解明された。
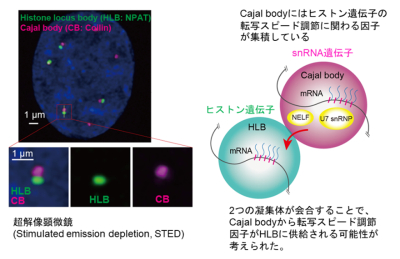
 図1:Pol IIがポリA鎖の無いヒストンRNAを正確に産生するために、MED26とLECはヒストン遺伝子(HLB)を転写するPol IIをCajal bodyに“ピットイン”させる
図1:Pol IIがポリA鎖の無いヒストンRNAを正確に産生するために、MED26とLECはヒストン遺伝子(HLB)を転写するPol IIをCajal bodyに“ピットイン”させる
メディエーター複合体のサブユニットMED26とLECは、核内凝集体Histone locus body(HLB)にCajal bodyを会合させることで、HLB内にあるヒストン遺伝子の転写の最終段階でPol IIを一時停止させ、適切なポリA鎖(ポリアデニル鎖)の無いヒストンRNAの産生に働く。
研究背景
DNAからなる遺伝子の情報は、転写と呼ばれるプロセスによってRNAに変換され、さらにRNAの情報は翻訳のプロセスによってタンパク質に変換されて遺伝子は機能を発現(発揮)します。この流れを遺伝子発現と呼びますが、遺伝子発現の制御機構の破綻は、がんや神経変性疾患などの様々な疾患発症の重要な要因となります。遺伝子発現制御で中心的な役割を果たす“転写”では、さまざまな転写調節因子の働きによってRNA合成酵素のRNAポリメラーゼII(Pol II)が遺伝子領域に呼び込まれ、RNA合成が開始(転写開始)されます。転写開始までに遺伝子領域に呼び込まれるPol IIの量が決定されるため、従来はこの過程が遺伝子発現の量を決定する上で最も重要であると考えられてきました。ところが、近年のゲノムワイドな解析により、Pol IIは転写開始後に、RNAを20~50塩基合成したところで一時停止することがわかり、遺伝子発現の調節で転写開始後のPol IIの転写速度(スピード)調節(転写伸長・転写終結の制御)が重要な役割を果たすことがわかってきました。
これまでに高橋教授の研究グループは、メディエーター複合体と呼ばれる巨大な転写制御複合体が、そのサブユニットMED26によって、Pol IIのスピードを調節する複合体Super elongation complex(SEC)やLittle elongation complex(LEC)をそれぞれ異なる遺伝子領域に呼び込んで、Pol IIの転写スピードを制御する仕組みを明らかにしてきました【Takahashi H et al, Cell 2011】【Takahashi H et al, Nat Commun 2015】。また、Pol IIによって合成されるほとんどのRNAは、その末端にポリA鎖(ポリアデニル鎖)が付加され、RNAは分解から保護されます。ところが、MED26とLECは、複製依存的ヒストン遺伝子*4(ヒストン遺伝子)やsmall nuclear RNA(snRNA)遺伝子などの特殊な遺伝子で、ポリA鎖が付加されないRNAの産生を促進することがわかりました【Takahashi H et al, Nat Commun 2020】。
この時、MED26とLECが転写の最終段階でPol IIの転写スピードを調節し、ポリA鎖のないRNAを産生する詳細な機構について明らかとなっていませんでした。また、ヒストン遺伝子とsnRNA遺伝子は、それぞれ細胞の核の中の“場”である核内凝集体 Histone locus body(HLB)とCajal body(CB)において転写されることがわかっていました。しかも、CBにはヒストン遺伝子の転写スピード調節に関わる因子(U7 snRNPやNELFなど)が集まっており、さらに、CBとHLBはいつも隣り合って会合することがわかっていました。このことから、ヒストン遺伝子を含むHLBにCBが引き寄せられることによって、ヒストン遺伝子の転写スピードが制御される可能性が予想されました(図2)。
図2:細胞の核内でHLBとCBは会合(隣接)して存在している
CBにはヒストン遺伝子の転写スピード調節に関わる因子(U7 snRNPやNELFなど)が集まっていることから、ヒストン遺伝子を含むHLBにCBが引き寄せられることによって、ヒストン遺伝子の転写スピードが調節される可能性が考えられた。
研究内容
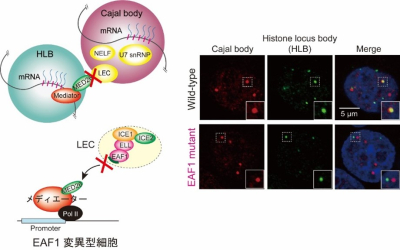
本研究で、MED26を含むメディエーター複合体とLECが、ヒストン遺伝子を含むHLBにCBを引き寄せることで、ヒストン遺伝子の転写の最終段階でPol IIのスピードを制御することが明らかになりました。MED26とLECの相互作用を欠失させ、その協働機能を喪失させた変異型細胞を作製し解析を行ったところ、HLBとCBの会合が著しく低下すると共に、ポリA鎖の付加された異常なヒストンRNAが蓄積することがわかりました(図3)。
図3:MED26とLECの結合はHLBとCBの会合に必要である
LECのサブユニットであるEAF1を変異させることで、MED26とLECが結合できない(協働できない)変異型細胞を作製した。この変異型細胞では、HLBとCBの共局在化(会合)が顕著に減少した。
このことは、MED26とLECが協働して、HLB内のヒストン遺伝子領域にCBを引き寄せ、ヒストン遺伝子の転写の最終段階で転写スピードを適切に調節することを示唆しています。
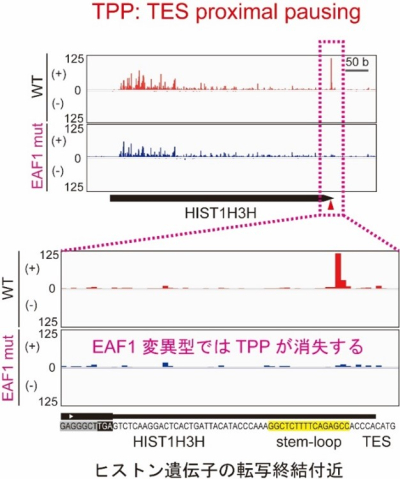
本研究グループはヒストン遺伝子の転写の最終段階で、Pol IIが一時停止することを発見し、この新規のPol IIの一時停止を“TPP”(TES proximal pausing)と名付けました(図4)。このTPPには、メディエーター複合体とLECとの協働が必要であり、CBとHLBの会合によってTPPが引き起こされることも明らかとなりました。このようにTPPは転写の最終段階でポリA鎖の付加を指令する配列の前にPol IIにブレーキをかけることで、RNAにポリA鎖が付加されないように適切に調節する「ピットイン」のような役割を果たしていると考えられます。
図4:ヒストン遺伝子におけるPol IIの新規の一時停止"TPP"
ヒストン遺伝子の転写終結付近で、新規のPol IIの一時停止"TPP"(顕著なピーク)が認められた。MED26とLECが協働できない変異型細胞ではTPPが消失することから、メディエーター複合体とLECの協働によってTPPが引き起こされることが示唆された。
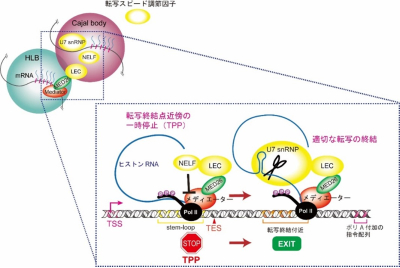
このようにMED26を含むメディエーター複合体とLECは、HLBにCBを会合させることでヒストン遺伝子の転写の最終段階でPol IIにブレーキをかけ、ポリA鎖の無いRNAを適切に産生することが明らかとなりました(図5)。
図5:メディエーター複合体と核内凝集体による転写終結制御のモデル
メディエーター複合体とLECの協働によってHLBとCBが共局在化(会合)することでTPPが誘導され、ヒストン遺伝子の適切な転写終結が制御されている。
今後の展開
遺伝子の転写終結の分子機構には未解明な部分が多く残されています。今回の研究で、転写終結に関与するPol IIの新たな一時停止機構が明らかとなったことにより、転写終結の制御機構のさらなる解明につながることが期待されます。また、MED26とLECが標的とする複製依存性ヒストン遺伝子やsnRNA遺伝子の発現制御機構は、腫瘍性疾患や知能障害、さらには神経変性疾患などの疾患とも深く関連しているため、本研究が疾患発症メカニズムの解明につながることも期待されます。
研究費
本研究は、文部科学省科学研究費補助金(高橋秀尚:17K19578, 18H02378, 19K22401, 21H05159, 21H02405, 21K19356、鈴木秀文:2020K15718)の研究費、ゲノム支援(221S0002)・先進ゲノム支援(16H06279)による支援、武田科学振興財団、寿原記念財団、高松宮妃癌研究基金、日本白血病研究基金、金原一郎記念医学医療振興財団、小野がん研究助成基金、小林がん学術振興会、MSD生命科学財団、内藤記念科学振興財団、上原記念生命科学財団、東京生化学研究会、中谷医工計測技術振興財団、横浜総合医学振興財団による助成金により行われました。
論文情報
タイトル: The 3' Pol II pausing at replication-dependent histone genes is regulated by Mediator through Cajal bodies’ association with histone locus bodies
著者:Hidefumi Suzuki†, Ryota Abe†, Miho Shimada, Tomonori Hirose, Hiroko Hirose, Keisuke Noguchi, Yoko Ike, Nanami Yasui, Kazuki Furugori, Yuki Yamaguchi, Atsushi Toyoda, Yutaka Suzuki, Tatsuro Yamamoto, Noriko Saitoh, Shigeo Sato, Chieri Tomomori-Sato, Ronald C. Conaway, Joan W. Conaway, Hidehisa Takahashi*
掲載雑誌:Nature Communications
DOI: 10.1038/s41467-022-30632-w.
用語説明
*1 メディエーター複合体:
31種類のサブユニットからなる巨大な転写制御複合体。さまざまな調節因子と相互作用することで、遺伝子発現の制御に重要な役割を果たす。
*2 Little elongation complex(LEC):
ICE1、ICE2、ZC3H8、ELL、EAF1からなる転写伸長因子複合体。snRNAとヒストン遺伝子の転写制御に働くことがわかっているが、LECの転写制御機構については未だに不明な点が多い。
*3 核内凝集体:
核内にはCBやHLBをはじめとした様々な凝集体が存在しており、それぞれが異なる機序で遺伝子発現制御に役割を果たしていると考えられている。近年の研究から、多数のタンパク質分子に加えて、様々なRNA分子が核内凝集体を構成していることがわかってきている。
*4 複製依存的ヒストン遺伝子:
DNAはヌクレオソームに巻きつくことで核内にコンパクトに収納されている。ヒストン遺伝子は、ヌクレオソームを構成するヒストンタンパク質をコードする遺伝子である。ヒトでは1番染色体と6番染色体に合わせて50個以上のヒストン遺伝子が並ぶ遺伝子クラスターを形成しており、細胞周期の複製期(S期)に特異的に転写・翻訳される。
参考文献など
本研究は、横浜市立大学大学院医学研究科 分子生物学の阿部 竜太共同研究員(研究当時:医学部学生)、嶋田 美穂客員講師、廣瀬 智威講師、廣瀬 博子氏、野口 慶介氏、池 陽子氏、安井 七海氏、古郡 華月氏、東京工業大学・生命理工学院の山口 雄輝教授、国立遺伝学研究所・比較ゲノム解析研究室の豊田 敦特任教授、東京大学大学院新領域創成科学研究科・メディカル情報生命専攻生命システム観測分野の鈴木 穣教授、がん研究会がん研究所・がん生物部の山本 達郎研究員、斉藤 典子部長、ストワーズ医学研究所の佐藤 チエリ博士、佐藤 茂生博士、Ronald Conaway教授、Joan Conaway教授のご協力を得て行われました。