藤田医科大学医学部生化学 下野洋平教授、医学部病理学 浅井直也教授、臨床腫瘍科 河田健司教授らの研究グループは、肥満が乳がんの促進因子であることに着目し、乳腺にある脂肪細胞が乳がん細胞に及ぼす影響を解析しました。この結果、脂肪細胞が十分脂肪を溜め込むほど発達(成熟)すると、乳がんを促進するタンパク質がより多量に分泌されて、乳がん細胞の浸潤や転移が格段に促進されることを明らかにしました。
成熟した脂肪細胞ががんを悪性化させる機構を示した本研究の成果により、今後、肥満ががんの危険因子となる仕組みの解明や、脂肪細胞の分泌因子の働きを抑えることで乳がんの進展を防ぐ全く新しい機構の抗がん治療の開発につながることが期待されます。
本研究成果は、英国の学術ジャーナル「サイエンティフィック・リポーツ」(8月9日号)で発表され、併せてオンライン版も同日に公開されています。
論文URL :
https://www.nature.com/articles/s41598-024-69476-3
<研究成果のポイント>
- 脂肪細胞の発達(成熟)によりがん浸潤が強力に促進されることを世界で初めて発見
- 脂肪細胞の成熟※1により分泌される免疫分子アディプシン※2および肝細胞増殖因子(HGF)が乳がん細胞の悪性化を促進することを証明
- 肥満が乳がんを悪性化させる分子機構を示唆
<背 景>
肥満は食道がん、膵臓がん、大腸がん、閉経後乳がん、子宮内膜がん、腎臓がんなど様々ながんの発生や進展の危険因子である。また、乳腺に豊富に存在する脂肪組織は、正常乳腺や乳がんの形成に必須の基盤となるとともに、乳がんの悪性化にも関与していると推測されてきた。研究グループは、乳がん手術検体を用いた解析から、乳腺脂肪細胞が分泌する免疫分子アディプシンががん細胞の増殖やがん幹細胞性※3を促進することを解明してきた(Goto H et al. Oncogene, 2019; Mizuno M et al. Cancers, 2021など)。しかし、乳腺脂肪細胞やその成熟ががん浸潤や転移などを促進する分子機構は不明である。
<研究手法・研究成果>
乳腺脂肪組織から分離培養した乳腺脂肪細胞が乳がん細胞の浸潤能に及ぼす影響を解析した。脂肪滴を十分溜め込むまで発達(成熟)した脂肪細胞は、未発達の脂肪細胞の10倍以上強く乳がん細胞の浸潤を促進した (
図1)。
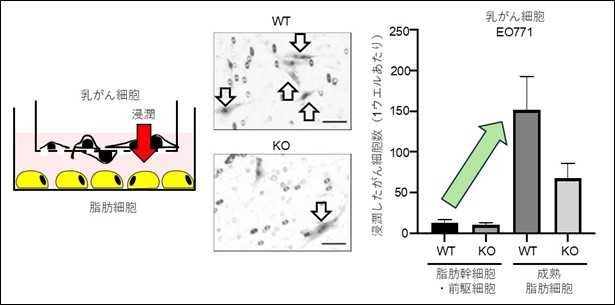
図1. 未成熟の脂肪細胞(幹細胞・前駆細胞)に比べ成熟した脂肪細胞は10倍以上強力に乳がん細胞(EO771)の浸潤を促進した(緑矢印)。
左: 実験のイメージ図。脂肪細胞のある区画に向かい浸潤したがん細胞数を測定する。
中: 浸潤したがん細胞(白矢印)、横棒: 50 マイクロメートル相当。
右: 浸潤したがん細胞数の計測。
WT: 野生型脂肪細胞、KO: アディプシン発現欠損(KO)脂肪細胞
脂肪組織は単なる余剰エネルギーの蓄積場所ではなく、内分泌器官としてさまざまな因子を分泌して食欲や代謝、炎症反応などを制御する。そこで、がん細胞の移動や浸潤の促進にも成熟した脂肪細胞の分泌因子が関わっている可能性を考え、成熟脂肪細胞が分泌する因子111種をスクリーニングした。その結果、免疫分子アディプシン、肝細胞増殖因子(HGF)などが脂肪細胞の成熟に伴い分泌されることが分かった。成熟した脂肪細胞から多量に分泌されるアディプシンは脂肪細胞を自己刺激して、脂肪細胞からのHGFなどの分泌をさらに促進した。このようにして成熟脂肪細胞から分泌されるアディプシンとHGFは協調して強力に乳がん細胞の移動、浸潤を促進した(
図2)。
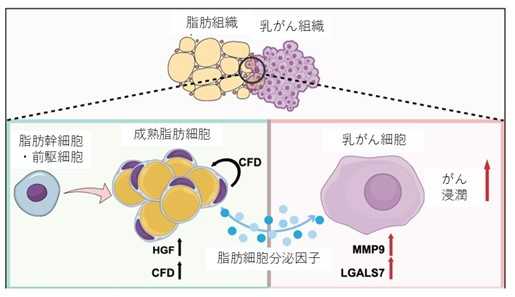
図2. 幹細胞・前駆細胞から発達し成熟した脂肪細胞ではアディプシン(CFD)の発現と分泌が急増し、その自己刺激作用により脂肪細胞からの肝細胞増殖因子(HGF)分泌が促進される(左下パネル)。これらの分泌因子が乳がん細胞を刺激してマトリックスメタロプロテアーゼ9(MMP9)やガレクチン7(LGALS7)の発現を誘導し、乳がん細胞の浸潤能を高める(右下パネル)。
これらの成果を踏まえ移植実験をしたところ、アディプシン遺伝子を欠損するノックアウト(KO)マウスでは、乳がんに接する乳腺脂肪組織へのがん細胞浸潤や炎症反応、腫瘍被膜形成が野生型マウスに比べ明らかに抑制されるとともに(
図3)、肺への乳がん転移を起こすマウスの数も減少した。その分子機構を解明するために腫瘍組織の遺伝子発現解析や、脂肪細胞とがん細胞の共培養実験を行ったところ、アディプシンを発現する成熟脂肪細胞は、がんの移動、浸潤、転移を促進するマトリックスメタロプロテアーゼ9やガレクチン7のがん細胞での発現を誘導することが分かった(
図2)。
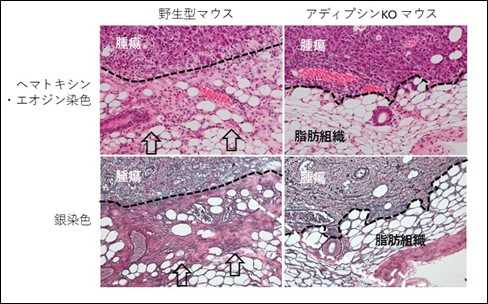
図3. アディプシンは乳腺腫瘍周囲の炎症反応、がん細胞浸潤や被膜形成を誘導する。
左:正常(野生型)のマウスに形成された腫瘍では腫瘍と乳腺脂肪組織の境界部に高度の腫瘍被膜形成とともにがん細胞浸潤や炎症反応がみられる。
右:アディプシンを発現しない(KO)マウスでは、これらの所見がほとんど見られなかった。
点線:腫瘍と脂肪組織の境界、白矢印:腫瘍被膜
<今後の展開>
脂肪細胞の成熟が乳がん細胞を一層悪性化させる分子機構を示した本研究は、肥満ががんの悪性化因子となる仕組みとも関連する可能性がある。今後、アディプシンやHGFなど成熟した脂肪細胞が分泌する因子を標的としたがん治療法の開発や、肥満を背景に発生および悪化する乳がん以外の各種のがん(食道がん、膵臓がん、大腸がん、子宮内膜がん、腎臓がんなど)の悪性化メカニズムの解明が進むことが期待される。
<用語解説>
※1 脂肪細胞の成熟:
脂肪組織形成のもととなる幹細胞・前駆細胞は脂肪滴を溜め込んではいないが、これらの細胞が分化する過程では細胞内に多数の脂肪滴を形成する。「脂肪細胞の成熟」は細胞内に多数の脂肪滴を溜め込んで最終分化するまで発達した状態をいう。
※2 アディプシン:
病原体を排除する自然免疫系で働く補体分子の一員。アディプシンは補体のD因子として補体系の活性化に働く。一方、アディプシンはその反応の副産物である補体C3aを介して、がん細胞の活性化にも働く。
※3 がん幹細胞性:
がん幹細胞は、がん組織に存在する多様ながん細胞をつくる大もととされる細胞である。「がん幹細胞性」はがん幹細胞のみがもつ、がん幹細胞の維持に必須の性質とされる。がん幹細胞は、がん細胞の「親玉」として特に高い腫瘍形成能力や治療抵抗性を持つため、がん幹細胞を標的にできれば、より有効ながん治療が可能になると期待されている。
<文献情報>
●論文タイトル
Adipsin-dependent adipocyte maturation induces cancer cell invasion in breast cancer
●著者
吉田淳平1,2、 林孝典1、 宗綱栄二1、 ベフヌーシュ ハレディアン1、 末石布志子1、 水野真広1、 前田真男1,3、 渡邊崇4、 牛田かおり3、 杉原英志4、今泉和良5、河田健司2、 浅井直也3、 下野洋平1
●所属
1藤田医科大学 医学部 生化学
2藤田医科大学 臨床腫瘍科
3藤田医科大学 病理学
4藤田医科大学 腫瘍医学研究センター
5藤田医科大学 呼吸器内科学
●DOI
10.1038/s41598-024-69476-3